SUA: J&J solicită aprobare, în regim de urgenţă, pentru vaccinul său anti-Covid
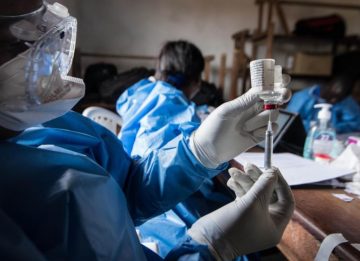
Compania Johnson&Johnson a solicitat, joi, autorizarea în regim de urgenţă pentru vaccinul dezvoltat împotriva infecției cu SARS-CoV-2.
Un răspuns al Administraţiei pentru Alimente şi Medicamente (Food and Drug Administration) este așteptat în săptămânile următoare.
Dacă va primi undă verde de la FDA, serul J&J va deveni al treilea autorizat în SUA, după cele ale Pfizer/BioNTech şi Moderna.
În faza a treia a studiilor clinice, vaccinul-candidat a prevenit spitalizarea şi decesul tuturor subiecţilor, la patru săptămâni după administrare, a anunţat compania săptămâna trecută. Efectele au fost observate, totodată, la persoane infectate cu variantele virusului descoperite iniţial în Marea Britanie şi Africa de Sud.
Dezvoltat de Johnson & Johnson în parteneriat cu Janssen Pharmaceuticals, vaccinul necesită refrigerare obişnuită şi se administrează într-o singură doză.
Cele ale Pfizer/BioNTech şi Moderna, precum şi cele dezvoltate de Oxford-AstraZeneca şi Novavax, sunt administrate în două doze.
Vaccinul Johnson & Johnson foloseşte un virus gripal comun inactiv (adenovirus), care învaţă sistemul imunitar să detecteze şi să lupte cu SARS-CoV-2, coronavirusul ce provoacă boala Covid.
Pfizer/BioNTech şi Moderna au folosit material genetic (ARN mesager) pentru a antrena sistemul imunitar în fața infecției.















